什么是诱导性多能干细胞?
What are iPSCs?
什么是诱导性多能干细胞?
What are iPSCs?
什么是诱导性多能干细胞?
诱导性多能干细胞 (英语: induced pluripotent stem cell, iPSCs) 简称为iPS细胞,由京都大学iPS细胞研究所的山中伸弥教授开发,其研究成果获得2012年诺贝尔生理学或医学奖。iPS细胞是指通过病毒载体等将特定的转录因子转入成体细胞(如皮肤或血细胞)使其重编程而成的多能干细胞。
诱导性多能干细胞的主要特征
通过利用以下的三个特征,培养足够数量的iPS细胞,并将其分化为神经元、心肌细胞和T细胞等各类必要的细胞,然后用于再生医学和药物发现。通过使用自身iPS细胞进行移植治疗,规避免疫排斥的风险。
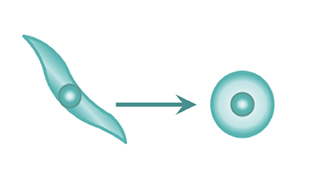
1. iPS细胞理论上能够由身体任何类型的细胞衍生
iPS细胞是通过将特定的转录因子转入血液、皮肤或毛发等不同类型的细胞并分化衍生而成。
1. iPS细胞理论上能够由身体任何类型的细胞衍生
iPS细胞是通过将特定的转录因子转入血液、皮肤或毛发等不同类型的细胞并分化衍生而成。
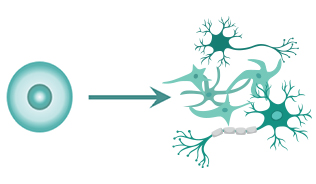
2. iPS细胞能够分化为各种器官组织的细胞
iPS细胞的主要特征是其多能性,即是细胞能够分化为神经元或心肌细胞等各种类型的细胞。
2. iPS细胞能够分化为各种器官组织的细胞
iPS细胞的主要特征是其多能性,即是细胞能够分化为神经元或心肌细胞等各种类型的细胞。
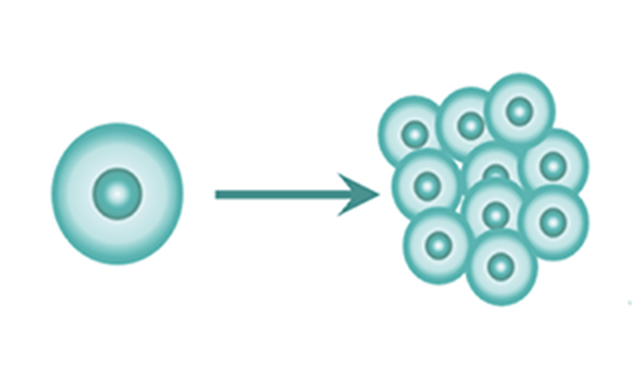
3. iPS细胞拥有近乎无限增殖的能力
iPS细胞能够通过细胞分裂来增加自身的细胞,以便获得所需的细胞数量。
3. iPS细胞拥有近乎无限增殖的能力
iPS细胞能够通过细胞分裂来增加自身的细胞,以便获得所需的细胞数量。
iPS细胞技术的应用实例
iPS细胞技术的应用案例大致分为两个方向。一个是从iPS细胞分化为神经元或肌细胞等特定的细胞类型并进行移植,即所谓的再生医学。另一个是利用患者细胞衍生的iPS细胞进行药物筛选或再现病理状况,以研究疾病机制。
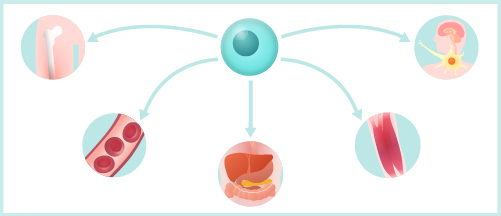
1. 应用于移植再生医学
再生医学使因受伤或疾病而受损的身体器官恢复功能。iPS细胞在理论上可以由身体的任何细胞衍生,并能分化为构成身体的各种细胞。iPS细胞拥有近乎无限增殖的能力,是细胞移植治疗的理想成体干细胞来源。iPS细胞的再生医学应用案例中,包括将iPS细胞的分化神经元移植到因车祸而造成脊髓损伤的病人体内,以恢复其瘫痪的肢体功能。此外,通过使用自身iPS细胞进行移植治疗,规避免疫排斥的风险。

2. 开发药物及调查病因
由患者血液等衍生的iPS细胞分化而来的神经元或心肌细胞等细胞,均带有相关疾病的信息。在培养皿上培养出带有疾病特征的细胞,以观察病理状况。换句话说,iPS细胞技术可以在培养皿中再现疾病状况,观察疾病的性质和机制,然后用各种候选药物的化合物处理细胞,在试管中确定其疗效和毒性。

自京都大学的山中伸弥教授在2007年宣布成功生成人类iPS细胞以来,国内外对其临床应用进行了各种研究。2017年开始了一项移植iPS细胞制备的视网膜色素上皮细胞的临床研究;2018年开始了一项将iPS细胞制备的多巴胺能神经元移植到帕金森病患者身上的临床试验,以及另一项将iPS细胞制备的心肌细胞片移植到严重缺血性心肌病患者体内的临床研究。日本厚生劳动省于2019年批准了一项将iPS细胞制备的神经祖细胞移植到脊髓损伤患者体内的临床研究计划。其他在糖尿病、角膜疾病、中风甚至肝脏和肾脏疾病方面的临床应用也正在研究之中。
CAR-T细胞疗法是另一个备受关注的癌症治疗研究领域。这个疗法是从癌症患者身上取出一种名为T细胞的免疫细胞,经过改造和增殖,然后放回体内攻击癌细胞。从iPS细胞作为病毒复制工具的角度来看,使用iPS细胞来研究疾病机制和开发新药有两个好处。首先iPS细胞技术可以用人类细胞进行研究;其次是iPS细胞可以无限增殖,以便获得所需的细胞数量。
研究人员调查疾病的原因或开发新药时,有时会从患者身上采集细胞等用作研究样本。然而,采集样本给患者造成不少负担,而且每次采集得到的细胞数量有限,以至能够进行的实验次数自然也不多。研究人员在研究领域上需要反复试错无数次来找出问题所在,并开发有效的药物。虽然使用实验动物的方法很常见,但始终动物与人类不同,在动物实验中有效的候选药物物质对人无效的情况并不少见。通过将由患者衍生的iPS细胞分化而来的细胞与动物实验相结合进行研究,有助在短时间内有效地开发新药,并更准确地评估药物的功效。此外,由于遗传背景和环境因素的差异,药物可能对每个人产生不同的效果和副作用,使用来自患者自身的iPS细胞将有助找出适合患者状态的最佳药物。特别是对于患者人数较少的难治性疾病的治疗药物,其开发成本逐年大幅增加,利用iPS细胞从而大大降低成本。
自京都大学的山中伸弥教授在2007年宣布成功生成人类iPS细胞以来,国内外对其临床应用进行了各种研究。
2017年开始了一项移植iPS细胞制备的视网膜色素上皮细胞的临床研究;2018年开始了一项将iPS细胞制备的多巴胺能神经元移植到帕金森病患者身上的临床试验,以及另一项将iPS细胞制备的心肌细胞片移植到严重缺血性心肌病患者体内的临床研究。日本厚生劳动省于2019年批准了一项将iPS细胞制备的神经祖细胞移植到脊髓损伤患者体内的临床研究计划。其他在糖尿病、角膜疾病、中风甚至肝脏和肾脏疾病方面的临床应用也正在研究之中。
CAR-T细胞疗法是另一个备受关注的癌症治疗研究领域。这个疗法是从癌症患者身上取出一种名为T细胞的免疫细胞,经过改造和增殖,然后放回体内攻击癌细胞。从iPS细胞作为病毒复制工具的角度来看,使用iPS细胞来研究疾病机制和开发新药有两个好处。首先iPS细胞技术可以用人类细胞进行研究;其次是iPS细胞可以无限增殖,以便获得所需的细胞数量。
研究人员调查疾病的原因或开发新药时,有时会从患者身上采集细胞等用作研究样本。然而,采集样本给患者造成不少负担,而且每次采集得到的细胞数量有限,以至能够进行的实验次数自然也不多。研究人员在研究领域上需要反复试错无数次来找出问题所在,并开发有效的药物。虽然使用实验动物的方法很常见,但始终动物与人类不同,在动物实验中有效的候选药物物质对人无效的情况并不少见。通过将由患者衍生的iPS细胞分化而来的细胞与动物实验相结合进行研究,有助在短时间内有效地开发新药,并更准确地评估药物的功效。此外,由于遗传背景和环境因素的差异,药物可能对每个人产生不同的效果和副作用,使用来自患者自身的iPS细胞将有助找出适合患者状态的最佳药物。特别是对于患者人数较少的难治性疾病的治疗药物,其开发成本逐年大幅增加,利用iPS细胞从而大大降低成本。
诱导性多能干细胞的发展
1958
成功开发青蛙体细胞核移植克隆技术
(约翰·伯特兰·格登爵士)
1998
建立人类胚胎干细胞系
2006
建立小鼠诱导性多能干细胞系
2007
建立人类诱导性多能干细胞系
2012
约翰·伯特兰·格登爵士/ 山中伸弥博士
获得诺贝尔生理学或医学奖
再生医療分野
2009
人类干细胞的首个临床试验许可
(胚胎干细胞/脊髓损伤)
2013
7月 年龄相关性黄斑变性临床试验获批 (全球首个诱导性多能干细胞)
2018
9月 血小板临床试验获批
11月 帕金森病移植手术首例
2019
2月 脊髓损伤临床试验获批
4月 年龄相关性黄斑变性移植手术5例术后1年随访结束
8月 角膜移植手术首例
12月 自然杀伤细胞的免疫细胞移植手术首例
2020
1月 软骨移植治疗临床试验获批
1月 心肌移植手术首例
創薬分野
2016
1月 脊髓性肌萎缩症临床试验开始
2017
8月 进行性骨化性纤维发育不良 临床试验开始
2018
4月 耳聋-甲状腺肿综合征临床试验开始
12月至今 肌萎缩侧索硬化症临床试验开始 (共3例)
1998
建立人类胚胎干细胞系
建立小鼠诱导性多能干细胞系
2006
2007
建立人类诱导性多能干细胞系
2009
人类干细胞的首个临床试验许可
(胚胎干细胞/脊髓损伤)
2012
约翰·伯特兰·格登爵士/
山中伸弥博士
获得诺贝尔生理学或医学奖
7月 年龄相关性黄斑变性临床试验获批
(全球首个诱导性多能干细胞)
2018
2013
9月 血小板临床试验获批
11月 帕金森病移植手术首例
2016
1月 脊髓性肌萎缩症临床试验开始
2017
8月 进行性骨化性纤维发育不良
临床试验开始
2019
2月 脊髓损伤临床试验获批
4月 年龄相关性黄斑变性移植手术5例
术后1年随访结束
8月 角膜移植手术首例
12月 自然杀伤细胞的免疫细胞移植手术首例
2020
1月 软骨移植治疗临床试验获批
1月 心肌移植手术首例
2018
4月 耳聋-甲状腺肿综合征临床试验开始
12月至今 肌萎缩侧索硬化症临床试验开始
(共3例)
